6. 全身オートラジオグラフィと TLC の定量解析に関する validation
ラジオルミノグラフィによる標識薬物の動態に関する多施設共同研究(薬物動態学会フォーラム 93)を振返って
田中 實,重松昭世*,長塚伸一郎**,中島栄一***
ヨーロッパ三共 Sankyo Europe GmbH, Dusseldorf(世話人代表)
*(株)生体科学研究所 270-1407 千葉県印旛郡白井町名内 340-2
**第一化学薬品(株)東海研究所 319-1182 茨城県那珂郡東海村村松 2117
***三共(株)分析代謝研究所 140-8710 東京都品川区広町 1-2-58
Key Words :
radioluminography,Imaging Plate,quantitative autoradiography,tissue concentration,distribution,radio-TLC,pharmacokinetics
Instruments for Radiation Measurement in Biosciences: Series 3. Radioluminography. 6. From the Collaborative Studies on Distribu-tion and Metabolism of Radiolabeled Drugs Using Radioluminography. Minoru TANAKA,Akiyo SHIGEMATSU*,Shin-ichiro NAGATSUKA** andEiichiNAKAJIMA***:SankyoEuropeGmbH,Immermannstrasse 45 40210 Dusseldorf F. R. Germany,*Institute of Whole Body Metabolism,340-2,Nauchi,Shiroi,Inba-gun,Chiba Pref. 270-1407,Japan,**Tokai Research Laboratories,Daiiti Pure Chemicals Co.,2117,Mura-matsu,Tokai-mura,Ibaraki Pref. 319-1182,Japan,***Pharmacokinetics and Drug Delivery Research Laboratories,Sankyo Co. Ltd.,1-2-58,Hiro-machi,Shinagawa-ku,Tokyo 140-8710,Japan.
文献請求先。 Corresponding author.
はじめに
本シリーズの前号1)に紹介されたように,定量的オートラジオグラフィ,特にラジオルミノグラフィ(RLG)技術の著しい進歩によって,日本のガイドラインの中に定量的オートラジオグラフィの活用が明記された。 すなわち,組織分布試験法に関しては,定量的オートラジオグラフィか組織計数法のいずれかでよく,望むらくは全身オートラジオグラフィ(WBA)法でのみ明示される詳細な分布パターンを定量的に評価するという新たな方向性が期待されることになった。
このような画期的な展開が実現されるに至った背景には,日本薬物動態学会フォーラム委員会(渡部 烈委員長)の要請を受けて,薬物動態談話会(加藤隆一会長)が世界に先駆けて「RLG という手法が薬物動態試験においてどの程度役立つのであろうか」 というテーマの多施設共同研究を実施したことが挙げられよう2)。 本共同研究は1992年10月に 21 の企業研究機関が参加して開始され,その最終報告は1993年10月の薬物動態学会フォーラム(フォーラム 93 と略)で公表,採択された。 本共同研究の大きな特徴は,その成果が,公正を期すために別に構成された 5 人の学識者(慶応大学加藤隆一,千葉大学佐藤哲男,東京大学杉山雄一,および東京薬科大学粟津荘司,渡部 烈の各教授)よりなる評価委員会に諮問され,学術的,中立的見地から RLG 法を薬物動態研究の新たな測定手法として適用しうるか否かが厳密に評価されたことである。
今号では,フォーラム 93 および同 proceeding(薬物動態,9,265-422(1994))2)に報告されたデータをもとに,RLG 法による WBA および TLC の定量に関する validation について考察する。
1. 共同研究の概要
1.1. 共同研究に参加した研究機関
次の各社が参加した。
旭化成工業, エーザイ, 大塚製薬, 鐘紡, 協和発酵工業, 三共, 塩野義製薬, 住友化学工業, 生体科学研究所, 第一化学, 第一製薬, 大正製薬, 大日本製薬, 武田薬品工業, 田辺製薬, 鳥居薬品, 帝人, 日本新薬, 日本たばこ産業, 藤沢薬品工業, 三菱化成。
参加は RLG 解析装置の有無にかかわらず任意とされており特に資格は設けられなかった。 また実験結果の表示には担当施設名は記載しないなどの配慮がなされている。 本共同研究には世話人代表として田中 實(薬物動態談話会幹事,三共)が就任し総括するとともに,作業の推進を補佐するための代表機関として第一化学(長塚伸一郎),生体科学(重松昭世)ならびに三共(中島栄一)が本研究における試料提供,データの集計,プロトコール案の作成や標準試料の提供などをサポートした。
1.2. 本共同研究で検討された項目
共通のプロトコールに基づいて実施された実験項目は次の 3 項目である。
(1) 第一段階として,同一 STD(ARC 社製,代表機関で nCi/g-organ に補正済)および全身切片試料(代表機関で作製)を回送して,各施設所有のバイオイメージングアナライザ(BA)装置による発光強度(PS△/mm2)が測定された(1992年11月~)。 STD の測定結果によって,同一放射線量で生じる発光強度は装置間でどの程度変動するかが検討された。
続いて,全身切片上の各組織の測定値では,読み取った発光強度値に見られる装置間の変動が,STD の測定値で補正した組織中濃度値で表すことによって,どの程度改善されるかを確認している。
(2) 第二段階として,実際に 14C 標識化合物をラットに投与し,投与後の 5 時点について組織中濃度を RLG 法あるいは臓器摘出法で定量する実験が行われた。 14C 標識化合物としては,生体内半減期が短く代謝を受けやすい indomethacin(IM)と,生体半減期が長く代謝を受けにくい chloramphenicol(CP)の 2 種が選ばれた。 参加した研究機関はあらかじめ IM および CP を担当するグループに分けられ,さらにその中で RLG と臓器摘出法の担当が割り当てられた(1993年 1 月~)。 BA の読み値を組織中濃度に換算するための標準試料は,第一段階で使用された STD が使用されている。
(3) 第三段階では,同一 TLC プレート(代表機関で作製)が回送され,放射能スポットの割合を各研究機関が測定して従来法(かきとり法: 代表機関で実施)で求めた割合と比較された(1993年 2 月~)。
2. プロトコールに見る実験計画の大綱
2.1. RLG 測定の施設間比較
標準線源,全身切片および TLC プレートの回送実験は担当グループを以下のように 2 グループに分けて実施された。 グループ分けの基準は地理的な至便性が配慮されたものである。
IM group 10 社: STD および第一化学より提供された 14C-IM 投与ラットの全身切片,ならびに同代謝物を展開した TLC プレートを回送
CP group 10 社: STD および生体科学より提供された 14C-CP 投与ラットの全身切片,ならびに同代謝物を展開した TLC プレートを回送
本実験で使用された STD は,5 桁の広い濃度範囲を持つ ARC-146C(American Radio-labeled Chemicals Inc.,USA)で,あらかじめ均一性を検定した 6 枚を選び,その 1 枚が 3 施設間で回送された。 また,全身切片はそれぞれの化合物を投与後 30 分の切片 6 枚(腎臓面 3 枚,正中線面 3 枚)が STD とともに担当施設に回送され発光強度が測定された。 この際,測定対照を統一するために切片の transparency copy に測定部位(ROI: region of interest)を図示したものが添付された。 測定対照組織は,心臓内血液,脳,顎下腺,肝臓,胸腺,肺,心筋,骨格筋,脾臓,膵臓,腎臓,精巣である。
組織内濃度への換算は,本シリーズの第 2 号3)に記載した方法に従って組織内濃度に補正した上記の STD を用いて行った。 すなわち,切片作製後のラット残体から肝臓,筋肉など均一断面をもつ組織を摘出し,LSC 計数法により求めた組織内濃度(nCig-organ)と,この切片の RLG で測定した同一部位の読取値(PSLmm2)とで得られた相関近似式によって行った。
測定条件は次のとおりである。
測定装置: 各機関が所有する BA(Model BA-100 および BAS-2000,Fuji Photo Film Co.,Ltd.)が使用された。
露出: 各機関で所有する Imaging Plate(IP と略す)を 15 分以上消去し,IM グループは 24 時間,CP グループは 6 時間露出した。 シールドボックスの使用は義務づけられていない。
読取り: 露出後の IP は試料と分離後 5 分以内に次の条件に従って読取りを行った。
画素サイズ(pixel size): 100μm
感度(sensitivity): 10000
ラチチュード(latitude): 4
階調数(resolution): 256 gradation
2.2. 体内分布実験
体内分布実験の担当グループを以下のように分け,実験は分担に応じてそれぞれの担当施設で独立に実施された。
IM group: RLG 法担当 6 社,LSC 法担当 5 社
CP group: RLG 法担当および LSC 法担当各 5 社
各社の分担は 1 施設当たり 1 時点各 1 動物で 5 時点を実施するものとされ,各社の負担を軽減するよう配慮されている。 できるだけ実験条件を統一するために動物のブリーダーなどが統一され,また投与薬物は担当全機関が同一ロットを入手できるようあらかじめアマシャム社の在庫が確保された。
データのまとめは(a)については第一化学が,(b)については生体科学がそれぞれ担当した。
(1) RLG 法によるラット組織内分布の測定
IM(比放射能; 3.7MBq/mg)および CP(比放射能; 7.2MBq/mg)を投与(1mg/kg)後,IM は 5,30 分,1,3,6 時間に,また CP は 5,30 分,6,24,48 時間に,非放血下でエーテル麻酔致死させ凍結した。
動物は Charles River 社の SD 系雄性ラット(体重 200g,6 週齢)を使用した。 切片の作製は各機関の定法にまかされ,切片の厚さは 30μm に指定された。 IP への露出は IM グループが 24 時間,CP グループでは 6 および 24 時間である。 測定対照組織は,LSC 法で採取可能な心臓内血液,脳,顎下腺,肝臓,胸腺,肺,心筋,骨格筋,脾臓,膵臓,腎臓,精巣が選ばれた。
(2) 臓器摘出法による組織分布の測定
投与,測定対象,測定時点等の条件は1と同じである。
所定時間後にラットをエーテル麻酔下に腹部下大動脈よりヘパリン血を採取し,ただちに各組織を採取した。 定法により処理したのち LSC 法によって放射能の計測が行われた。
2.3 TLC-RLG 法による代謝物の分離定量
IM(第一化学担当)および CP(生体科学担当)投与後のラット尿,プラズマおよび胆汁を TLC 展開し,上記のプロトコールに従って施設間で回送・測定された。 TLC は最終的に代表機関でスポットの LSC 測定が行われた。
3. STD および全身切片回送試験結果が示すもの
STD を施設間で回送・測定した結果(PS△/mm2)は,IM のグループ(表 1 )と CP のグループ(表 2 )では露出時間が異なるため別々の表にまとめてある。 同一放射能濃度に対して読み取られた発光強度は,大部分の施設では差はほとんど認められなかったが,一部施設間で差のあることが明らかになった。
一方,全身切片の回送実験では,指定された ROI を各機関で測定した結果(PS△/mm2)は同様に一部で施設間の差が見られた。 しかし,この値を STD の測定値で calibration して求めた結果(nCi/g-organ,表 3 )では,このような差が顕著に減少することが示されている。 同一放射能に対する装置の応答性に影響を与える要因として考えられるものは,フォトマルやレーザーの性能変化,ミラーの設置位置のずれ,温度など読取環境の違い,などさまざまである。 本実験において,これらのばらつきが STD で calibration することにより改善され,施設間整合性が得られることが確認された成果は大きい。
一方,本共同研究で明らかになったこのような装置間の感度差について,今後の課題としてさらに装置メーカーを含めた検討を加えるよう評価された。 この点に関してはラジオルミノグラフィ研究会で主催した装置の面均一性と直線性に関する validation 共同研究(1996年10月~1998年 4 月,本シリーズ第 4 号4)で紹介)で検討された結果,変動要因の多くはメーカーによるメンテナンスで改善されることが明らかにされた。 したがって,適当な保守点検を行うことで上記のばらつきはさらに減るものと思われる。
概括的には,いずれのグループにおいても測定の結果に大きな差は認められなかったことが指摘され,各施設での機器の設置条件その他の条件は測定結果に大きな影響は与えなかったことが明らかにされた。 しかしながら,低濃度域では測定値の CV が比較的高かったが,このことは同一施設内での繰返し測定でもみられることから,施設間の差に由来するものとは考えられず,測定値がバックグラウンドに近いことによるものと考察された。

拡大 |
表1 14C-スタンダードの各施設での実測値(indomethacinグループ)
PSL(-BG)/S
表2 14C-スタンダードの各施設での実測値(chloramphenicolグループ)
PSL(-BG)/S
|

拡大 |
表3 臓器中濃度で表した14C-スタンダードの各施設での実測値 |
4. RLG 法による体内分布実験の有用性
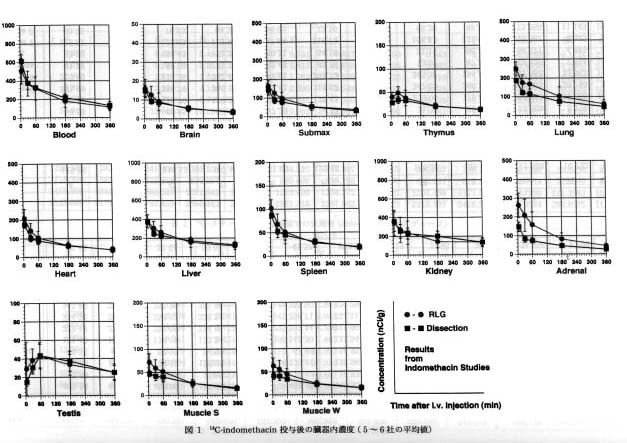
図 1 には IM の体内分布について,図 2 には,CP の体内分布について,RLG 法と LSC 法で測定された各臓器中濃度の経時変化が平均値で示されている。
各プロットは独立した機関で得られた n=1 のデータの平均値であるにもかかわらず,両薬物ともに大部分の臓器では二つの方法で得られた値はよく類似していた。 また,大部分の臓器は各時点でほぼ同程度の CV 分布が見られたが,一部で RLG 法がやや高い傾向が見られる臓器と,反対に LSC 法が高い CV を示す臓器があった。
RLG 法の CV に影響する要因として,切片厚の変動,切片の乾燥条件,ROI 設定の違い,などが挙げられるが,今回の実験では,乾燥条件についてはミクロトーム内部あるいは乾燥用フリーザなどで定法に従った乾燥が十分に行われたと考えられる。 また ROI 設定については,切片の回送実験で ROI のモデルが提供されており,プロトコールでも取決めがなされていることからそれほど大きな影響はないであろう。 一方,切片厚については設定(30μm)に関する装置間の整合性はあるとの前提で実施していることから,STD を組織中濃度にcalibrate する際に用いた切片厚と試料の切片厚が異なる可能性は否定できない。 しかし,この要因は同一ミクロトームで両切片を得ることで排除されるので,通常の測定では問題にならない。
今回の共同研究のプロトコールには,STD の calibration に関する事柄は含まれなかったが,CP のグループのうち数社において独立に切片採取後の残体の臓器を摘出して LSC 計数(x)が行われた。 RLG 計測値(y)は共同研究で用いた calibration curve によって換算したものであり,得られた両測定結果をみるとそれぞれの相関図は必ずしも y=x にあてはまらないことがわかった。 LSC 計測に問題がなければこの傾きの違いは各機関ごとに RLG のcalibration を行う必要性をさらに強く示唆するものとなっている。
一方,投与初期においては RLG 法がやや高い傾向が示されたが,2 時間以降では両測定値はほとんど同じ結果が得られている。 特に IM では肺と副腎が,また CP では肺が両手法で異なる値が測定されており,前者は RLG 法の測定値がやや高く,後者はやや低い傾向が見られた。 これらの原因は一部の臓器で固有の calibration の必要性を示しているとともに,LSC 法が放血後にサンプリングをしているのに対して,RLG 法では血液を含んだ状態で測定値を得ていることから,血管分布の多い臓器では血中濃度の影響を受ける可能性があり,別に行われた放血後の RLG 実験でこのことが確認されている。
拡大 |
図1 14C-indomethacin投与後の臓器内濃度(5-6社の平均) |

拡大 |
図2 14C-chloramphenicol投与後の臓器内濃度(6社の平均) |
5. TLC による代謝物の分離定量の有用性
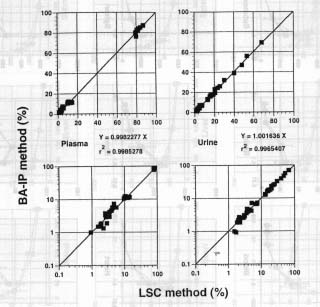
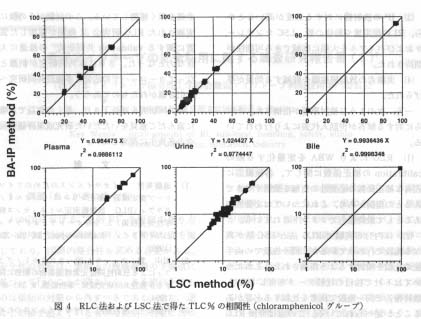
RLG および LSC 両手法で得た TLC% が図 3 および図 4 に比較されている。
IM,CP ともに結果は多施設相互できわめてよい相関性が示されており,代謝物測定に RLG 法を利用することはきわめて有用であることが明らかにされた。 むしろ,かきとりによって生ずる誤差を避けることができるという大きな利点があり,今後有効に活用されることが望まれている。
RLG 法で TLC を解析する方法はすでに定法として広く実施されており,本共同研究で改めて施設間の再現性が確認された。 しかし,本シリーズ第 2 号3)で詳述したように,生体成分など夾雑物を多く含む試料ではラジオスポットの明確な分離測定が困難であり精製が必要であることや,高感度な IP では低レベルのプレートの汚染が検出され実際のスポットとの識別が難しく面均一性や IP の汚染チェックが必要であることは言うまでもない。
拡大 |
図3 RLC法およびLSC法で得たTLC%の相関性(indomethacinグループ) |
拡大 |
図4 RLC法およびLSC法で得たTLC%の相関性(chloramphenicolグループ) |
6. RLG 法に対する評価委員会の評価
本共同研究の最終報告に対しての評価委員会の見解がフォーラム 93 で渡部 烈フォーラム委員長から発表5)された。 その大綱は,RLG 法が注意深く実施されるとき,従来の手法と等価な成績を与えるのみならず,いくつかの点で優れていることが立証されたものと評価された。 したがって RLG 法を単に従来法の代替法と位置づけるのではなく,今後の薬物動態研究に関するより高度な情報を取得する手段として積極的に活用することが望まれている。
共同研究の成果に対する評価の概要は以下のとおりである。
(1) RLG を WBA の定量に適用することにより,一般的な体内分布が得られるほか,組織内の詳細な定量的知見が得られ,これらを画像として視認できる点が特に評価された。 そしてこれにより従来法に比べて薬物の体内分布と薬効,毒性発現の関連性をより客観的かつ動的に究明できる可能性が期待された。
(2) TLC への応用では,従来法に比べて代謝物の経時追跡操作が容易であり,結果の定量性がより高くかつ客観性に富むことを指摘している。
(3) IP の放射線に対する感度が高いことから,RI の使用量や動物の数,LSC シンチレータおよびバイアルを大幅に削減できる可能性が期待された。
(4) 実験者の放射線被曝を軽減する効果が挙げられた。
一方,次のような検討事項が指摘され,それらに対する解答が世話人代表により行われている。
(1) RLG により WBA を定量化する際の calibration の補正係数に関して,各種臓器に固有な補正係数の必要性の有無を検討すべきであるとの指摘があり,これについては必要性があるとして最終報告でコメントされている。
(2) 体内分布実験で RLG 法と LSC 法が異なる施設で行われているが,同一施設での両手法の比較を検討するよう指摘された。 これについては 6 社で独自の比較データを有しており,最終報告で同一施設で両者を比較する必要があることが述べられている。 この点は今後 RLG 研究会等でさらに検討を加える予定である。
お わ り に
21 の製薬メーカー研究機関が参画して,1 年にわたって実施された大規模な共同研究について,薬物動態2),5)に報告された内容をもとに概観した。 プロトコールに盛り込まれた検討事項に明らかなように,種種の制約に阻まれながらも参画され,多くの成果をもたらされた参加機関の担当者各位に深く敬意を表したい。 サポート役の一人として至らぬ点の多きことを心からお詫びするとともに,貴重な機会に参加できた幸運を深く感謝している。 この経験がその後に実施された RLG 研究会 31 機関が参加した装置に関する validation 共同研究4)の推進に大きな力となった。 さらに本共同研究が刺激となってヨーロッパでの活発な多施設共同研究へと引き継がれたものであろう。
本共同研究を評価下さり,多くの有益で示唆に富んだご意見をいただいた研究成果評価委員会の各先生に深謝したい。
文 献
1) 進藤英世: バイオサイエンスのためのアイソトープ測定機器: 第三シリーズ ラジオルミノグラフィ(RLG,放射線測定ルミネッセンス輝尽性発光技術)5. 全身オートラジオグラフィとガイドライン,Radioisotopes,48,216-226(1999)
2) 田中 實: フォーラム 93―ラジオルミノグラフィによる放射性同位元素標識薬物の動態に関する多施設共同研究成果,薬物動態,9,393-407(1994)
3) 中島栄一,河合賢司: バイオサイエンスのためのアイソトープ測定機器: 第三シリーズ ラジオルミノグラフィ(RLG,放射線測定ルミネッセンス輝尽性発光技術)2. ラジオルミノグラフィによる放射能測定の一般的技術に関して,Radioisotopes,47,953-965(1998)
4) 長塚伸一郎: バイオサイエンスのためのアイソトープ測定機器: 第三シリーズ ラジオルミノグラフィ(RLG,放射線測定ルミネッセンス輝尽性発光技術)4. 装置の面均一性と測定値の直線性のバリデーション,Radioisotopes,48,132-145(1999)
5) 渡部 烈: 「フォーラム 93」 新医薬開発にかかわる諸問題―ラジオルミノグラフィー(RLG)は薬物動態研究にどこまで役立つか,薬物動態,9,351-353(1994)
|

